缺血性腦損傷會引發一系列復雜的基因表達、分子信號、細胞機制及電生理活動,這些過程促進大腦皮層的功能重塑與突觸再生,構成卒中后自發恢復的神經生物學基礎。研究表明,卒中后兩周內實施康復策略與更有利的預后相關。
近日,首都醫科大學附屬北京天壇醫院的李子孝教授團隊,通過TMS-EEG技術,深入揭示了急性缺血性卒中后兩側大腦半球間的動態作用,發現健側初級運動皮層(primary motor cortex, M1)對患側M1的β頻段神經振蕩具有抑制作用,而這種抑制與運動功能障礙程度及后續恢復密切相關。
該發現進一步印證了“半球間競爭”模型在卒中恢復早期階段的作用機制,提示調控β振蕩可能成為新型神經調控干預的重要方向。

一、研究方法
1.研究對象
單中心病例對照研究(2022年12月至2024年5月,首都醫科大學附屬北京天壇醫院神經內科)
19例癥狀出現14天內確診的缺血性卒中患者
(平均年齡為47.95±12.41歲;15例為男性)
16名年齡和性別匹配的健康對照者
(平均年齡為53.56±9.83歲;12名為男性)
納入標準
(1) 年齡在18至80歲之間
(2) 經擴散加權磁共振成像證實為單側缺血性腦卒中
(3) 卒中發作時間在14天以內
(4) 存在單側上肢運動功能障礙
排除標準
腦卒中患者:存在TMS或MRI禁忌癥、雙側腦梗死、腦出血、認知障礙或因失語而無法簽署知情同意書的患者。
健康對照組(healthy control, HCs):存在神經系統或精神疾病病史、運動障礙,或存在TMS或MRI的禁忌癥。
2.研究設計
(1)功能評估
入組后48小時內,評估卒中后基線功能狀態:
評估初始功能障礙程度
美國國立衛生研究院卒中量表(National Institutes of Health Stroke Scale, NIHSS)
輕度卒中定義為基線NIHSS ≤ 5
重度至中重度卒中定義為基線NIHSS ≥ 6.25
Fugl-Meyer運動功能評估(Fugl-Meyer assessment, FMA)
FMA上肢亞量表(FMA-upper extremity)評估初始功能障礙程度
評估患者日常生活活動能力
改良Rankin量表(modified Rankin Scale, mRS)和Barthel指數
評估癱瘓側上肢的肌張力
改良Ashworth量表
卒中3個月時重新評估NIHSS(NIHSS3m)和mRS(mRS3m)
NIHSS評分的變化(ΔNIHSSbaseline-3m)用于評估卒中后的恢復情況
(2)TMS-EEG
本研究采用8字形線圈(M-100 Ultimate;深圳英智科技有限公司,深圳,中國)進行聚焦磁刺激。
在TMS-EEG同步記錄過程中,使用實時神經導航系統(ROB 9000系列;深圳英智科技有限公司)結合每位受試者的T1加權磁共振成像掃描,對M1區域進行精準定位刺激。
頭皮腦電圖采用兼容TMS的Ag/AgCl燒結C環電極,通過彈性電極帽(EasyCap GmbH,德國)按照國際標準10-20電極系統放置,并連接TMS兼容的64通道腦電系統(actiCHamp Plus C;深圳英智科技有限公司)進行采集。

①運動熱點的確定
TMS線圈被定位于根據T1加權掃描圖像識別的手部運動區(hand knob region)的解剖標志周圍。
健側M1(contralesional M1, clM1)的運動熱點定義為:當TMS線圈以45°后-前方向貼近頭骨施加單次刺激時,在非癱手第一背側骨間肌誘發最大運動誘發電位(MEP)的線圈位置。
患側M1(ipsilesional M1, ilM1)的運動熱點定義為:基于個體T1加權掃描所識別的手部運動區。
②TMS-EEG方案
在腦電圖記錄期間,對運動熱點至少施加80次TMS脈沖,刺激強度為健側靜息運動閾值(resting motor threshold, RMT)的80%,刺激間隔為2.0-4.0 s。
對于卒中患者,單脈沖TMS先刺激健側M1(clM1),再刺激患側M1(ilM1)。
對于健康對照組,單脈沖TMS依次施加于優勢側M1和非優勢側M1。
③TMS-EEG實驗控制措施
為避免TMS引發的聽覺誘發電位以及因TMS點擊聲導致的眨眼和眼肌反應,要求受試者佩戴耳塞。
為進一步減小TMS引發的骨傳導影響,在TMS線圈與腦電電極帽之間置入一層薄塑料膜進行隔離處理。
3.數據分析
對腦電信號預處理后,計算M1區域的局部平均場強(local mean field power, LMFP)和功率譜密度(power spectral density, PSD)。
在健康對照中,M1的LMFP范圍為3-7 μV;在卒中患者中,患側M1的LMFP范圍為1.5-3.5 μV,而健側M1的LMFP范圍為4-8 μV。
LMFP在健康受試者和卒中患者之間差異顯著,特別是在25-35 ms時間窗內。因此選擇25–35 ms區間內的LMFP(LMFP25–35 ms)用于后續分析。
通過Morlet小波變換計算事件相關頻譜擾動(event-related spectral perturbation, ERSP)來評估時頻域中的頻譜特征。重點關注不同感興趣頻段:
δ(<4 Hz)
θ(4–8 Hz)
α(9–12 Hz)
β(13–27 Hz)
低γ(27–50 Hz)
高γ(>50 Hz)
采用Spearman相關分析法評估TMS-EEG指標與卒中后初期的功能損傷及3個月功能恢復之間的相關關系。
二、研究結果
1.基線特征
從開始到完成腦電圖檢查的平均時間為8.34 ± 2.31天。所有患者均為單側大腦半球缺血性梗死灶,且上肢肌張力正常(改良Ashworth量表評分為0)。
基線時運動障礙程度從輕度到重度不等,其中5例為輕度卒中,14例為重度卒中,11例患者完全喪失手部運動功能。
基線各項運動功能評估指標如下(數據為中位數 [四分位距]):
FMA總分:35 [19–49]
FMA上肢評分:12 [5–26]
NIHSS評分:7 [5–8]
mRS評分:3 [3–4]
Barthel指數:60 [50–75]
全部患者均完成了3個月隨訪:
NIHSS3m評分:3 [1–4]
mRS3m評分:1 [1–2]
2.缺血性腦卒中后皮層活動的特征
TEPs TMS誘發電位
在卒中后2周內評估TMS誘發腦電圖反應時,發現患側皮層與健側皮層在100 ms內的TMS誘發電位(TMS-evoked potentials, TEPs)表現出兩種不同特性:
在健康對照中,對M1施加TMS刺激可誘發具有正負偏轉的復雜TEPs波形變化。
相比之下,在缺血性腦卒中患者中,當TMS施加于患側M1時,其TEPs波形更為簡單;當TMS施加于健側M1時,其TEPs的正負偏轉幅度較低。
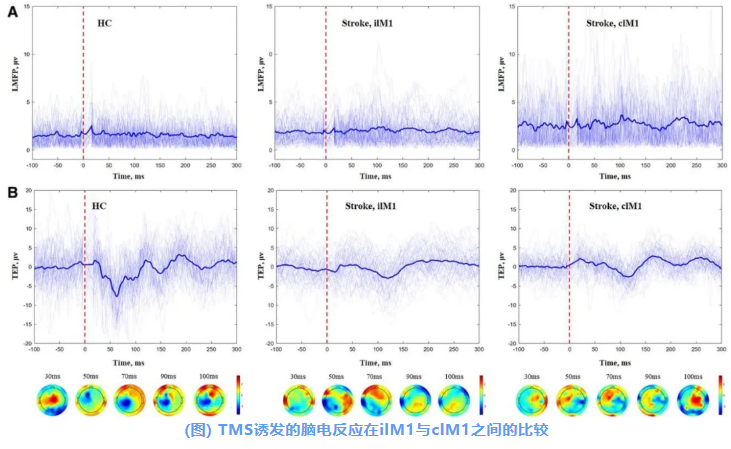
在圖中,以蝶形圖展示了一名代表性HC與一名卒中患者在患側M1與健側M1上的LMFP及TEPs;所有通道的信號均被展示,其中加粗的通道表示感興趣區域。
研究進一步探討了在100 ms時間窗內,TMS刺激健側M1對患側M1神經活動的影響:
在健康對照中,TMS刺激在對側M1區誘發了復雜的TEPs波形變化,表現為明顯的正負偏轉(圖A)。
然而,在卒中患者中,對健側M1施加TMS刺激時,患側M1的TEPs波形更為簡單(圖B);當TMS施加于患側M1時,健側M1誘發的TEPs仍表現為正負偏轉,但振幅較低(圖C)。

展示了一名代表性HC的M1 TEPs(圖A),一名代表性卒中患者在健側M1刺激下的患側M1 TEPs(圖B),以及一名代表性卒中患者在患側M1刺激下的健側M1 TEPs(圖C),均以所有通道的蝴蝶圖形式呈現(粗體通道代表感興趣區域)。紅色虛線表示TMS脈沖的時點。“ilM1_clM1tar”表示健側M1刺激下的患側M1 TEP。
RMT 靜息運動閾值
健康對照組的RMT為刺激器最大輸出的74.63±9.67%,而卒中患者的健側RMT為63.42±13.40%,二者差異具有統計學意義(t=?2.79;P=0.009;圖A)。
此外,在缺血性卒中患者中,健側RMT與患側M1的LMFP25–35 ms呈正相關(r=0.482;P=0.018;圖B)。
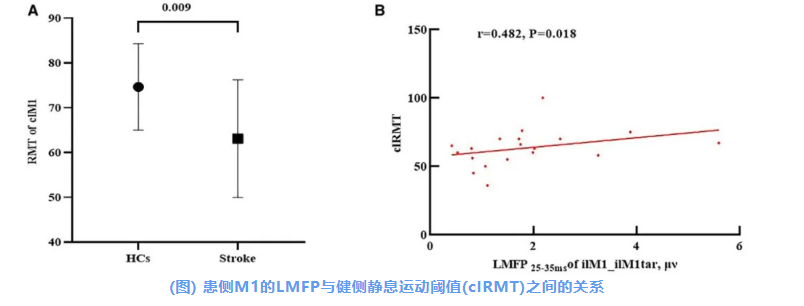
A:兩組之間健側RMT的比較。
B:卒中患者中,TMS刺激后25–35 ms內患側M1的LMFP與健側RMT之間的關系。
HC表示健康對照;LMFP25–35 ms表示TMS刺激后25到35 ms內的局部平均場強。
3.患側M1的TMS誘發振蕩頻率變化
ERSP 事件相關頻譜擾動
PSD 功率譜密度
在健康對照中,100 ms內M1的δ、θ、α、β及低-γ振蕩功率顯著增加(圖A)。輕度卒中患者在100 ms內α、β及γ振蕩功率增加(圖B);相反,中重度卒中患者在100 ms內β與γ振蕩功率減少(圖C)。
在分析各頻率下的PSD差異時,發現卒中組在37-44 Hz頻段存在顯著升高(圖D)。
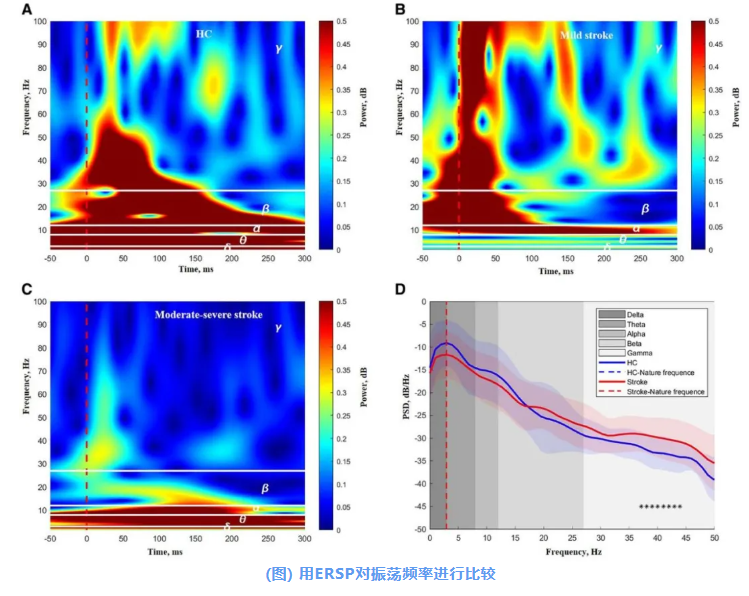
展示了相應的ERSP模式(頻率范圍在100 HZ以內):1名HC(A)、1名代表性輕度卒中患者(B)和1名代表性中重度卒中患者(C)。兩組之間的功率譜密度(PSD)比較見圖D。圖中紅色虛線(A-C)表示TMS脈沖的時點(*:P<0.05,未經多重比較校正)。
Spearman相關分析
研究進一步檢驗了患側M1中TMS誘發腦電活動的改變是否與卒中初期的功能損傷有關。β振蕩功率與NIHSS評分呈負相關,與Barthel指數評分呈正相關;γ振蕩PSD亦與Barthel指數呈正相關。
4.刺激健側M1對患側M1的影響
ERSP 事件相關頻譜擾動
PSD 功率譜密度
為進一步明確卒中患者中TMS誘發腦電響應的特征,研究提取了在健側M1 TMS刺激下的患側M1的振蕩頻率。
在健康對照中,TMS刺激后100 ms內,對側M1中δ、θ、α、β及低-γ振蕩功率顯著增加(圖A)。在卒中患者中,TMS刺激后100 ms內患側M1中的β和低-γ振蕩功率顯著下降(圖B&C)。
與健康組相比,卒中組在健側M1刺激下患側M1中16-17 Hz的β振蕩PSD顯著下降(圖D)。
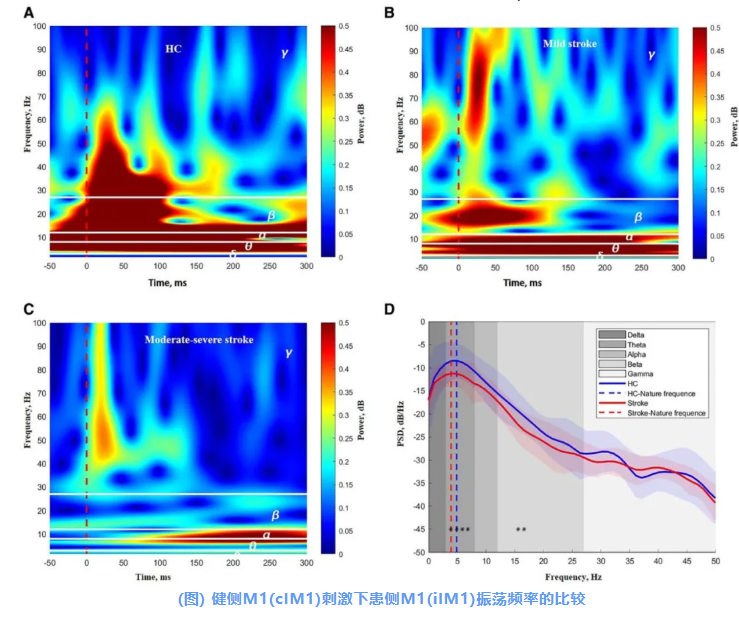
展示了相應的ERSP模式(頻率范圍在100 HZ以內):1名HC(A)、1名代表性輕度卒中患者(B)和1名代表性中重度卒中患者(C)。兩組之間的功率譜密度(PSD)比較見圖D。圖中紅色虛線(A-C)表示TMS脈沖的時點(*:P<0.05,未經多重比較校正)。
Spearman相關分析
研究進一步分析了健側M1刺激下患側M1的TMS-EEG指標與卒中后功能障礙和恢復的關系。
β振蕩功率與FMA評分(r=?0.557;P=0.014)及FMA上肢評分(r=?0.503;P=0.014)呈負相關(圖A&B)。而在刺激健側M1時,β振蕩功率與NIHSS評分變化呈正相關(圖C)。
類似地,β振蕩PSD與FMA評分呈負相關(r=?0.417;P=0.038;圖D),與FMA上肢評分也呈負相關趨勢(r=?0.389;P=0.05;圖E)。然而,β振蕩功率與NIHSS評分變化之間無顯著相關性(r=0.271;P=0.131;圖F)。

clM1 表示健側M1;ilM1_clM1tar 表示在刺激健側M1時患側M1的TEPs;ilM1 表示患側M1;PSD 表示功率譜密度。
三、研究討論與總結
本研究顯示,與健康對照組相比,急性缺血性腦卒中患者的患側M1神經活動顯著降低,而健側M1神經活動則顯著增強。在卒中患者中,健側M1的神經活動增強與患側M1的神經活動減少呈負相關。
患側M1中的β和γ振蕩活動增強,這一變化與卒中后的初始功能損傷程度呈負相關。而健側M1則抑制了患側M1的β振蕩活動,該機制與卒中后3個月的功能恢復較差相關。
神經可塑性在缺血性腦卒中的急性期開始顯現,并在亞急性期達到高峰,因此這一時期是神經調控干預的關鍵窗口。本研究中,健側M1對患側M1的神經活動具有抑制作用,證實在卒中急性期,“半球間競爭模型”在功能恢復中起主導作用。
本研究中,TEP的早期成分以及β和γ振蕩在卒中后均出現異常,提示興奮性與抑制性神經元之間的動態平衡被破壞。“半球間競爭模型”的潛在機制可能涉及健側大腦皮層通過影響皮層和皮下谷氨酸能或GABA能神經元的活動,來抑制患側運動皮層的興奮性。
高頻神經振蕩是促進神經元間信息交流和整合的重要機制,尤其是γ振蕩活動依賴于GABA受體介導的抑制作用,這表明高頻振蕩活動主要由抑制性中間神經元網絡產生。γ與β振蕩在運動控制和認知功能中發揮關鍵作用,其紊亂可能反映功能損傷及其對神經處理的影響。
卒中后,腦內神經振蕩活動受到干擾。在急性缺血性卒中中,患側M1的γ與β振蕩活動增強,并與卒中后的功能障礙嚴重程度相關。這一關聯強調了高頻振蕩活動作為卒中嚴重程度與疾病進展生物標志物的潛在價值。
研究總結
健側M1的興奮性增強與患側M1的興奮性降低密切相關,提示“半球間競爭模型”在急性缺血性卒中后的功能障礙與恢復中發揮主導作用。
健側M1對患側M1的β振蕩的調控作用,可作為卒中后功能障礙與恢復的生物標志物。通過調控健側M1以增強患側M1的β振蕩,可能是一種改善卒中后功能恢復的潛在策略。
聲明
此內容由英智科技臨床支持部整理,歡迎批評指正。轉載請注明出處。
參考文獻
Jia, W., Zhou, Y., Mao, J., Feng, J., Han, Y., Xu, F., Wang, X., Liu, T., & Li, Z. (2025). Inhibition of Ipsilesional M1 β Oscillations by Contralesional M1 Following Acute Ischemic Stroke: A TMS-EEG Study. Stroke, 10.1161/STROKEAHA.124.050376. Advance online publication. https://doi.org/10.1161/STROKEAHA.124.050376